Científicos de EE.UU. Han creado una terapia CAR-T que genera células inmunes en el interior del organismo, en lugar de hacerlo en laboratorio como hasta ahora. El avance puede ampliar las posibilidades de las terapias CAR-T actuales, al permitir que estos tratamientos lleguen a más pacientes, se extienda su uso a más enfermedades y se reduzcan sus efectos secundarios.
La opción de generar células CAR-T en el propio organismo es prometedora para el tratamiento de enfermedades autoinmunes, señalan los autores de la investigación en la revista Science, donde hoy presentan sus resultados. Estas enfermedades afectan a alrededor del 10% de la población mundial y actualmente no tienen curación.
El avance también podría ser útil para mejorar el tratamiento de cánceres hematológicos como algunas leucemias y linfomas, añaden los investigadores. Por ahora han probado la técnica con éxito en ratones y en macacos, y acaban de iniciar el primer ensayo en personas en Australia.
Alrededor del 10% de la población tiene alguna enfermedad en que el sistema inmune ataca por error el propio cuerpo
La investigación está coliderada por el inmunólogo Carl June, de la Universidad de Pensilvania, que desarrolló las terapias CAR-T para el cáncer y las utilizó para curar por primera vez a una paciente en 2012.
Estas terapias se han basado hasta ahora en extraer células inmunes de la sangre de un paciente y modificarlas para que reconozcan y ataquen las células del cáncer. Una vez modificadas, se llaman células CAR-T. Posteriormente, se multiplican en laboratorio para obtenerlas en grandes cantidades y se transfunden en el cuerpo de los pacientes.
Las terapias CAR-T han transformado el pronóstico de algunas leucemias y linfomas, pero hasta ahora se hacen a medida para cada paciente, lo que limita su uso, porque requiere tiempo, dinero y equipamiento. Además, deben acompañarse de un tratamiento de inmunosupresión que comporta un riesgo de efectos secundarios.
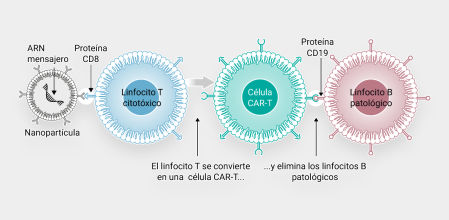
Para sortear estos obstáculos, investigadores de la Universidad de Pensilvania y de la biotec Capstan Therapeutics han creado nanopartículas lipídicas, que son pequeñas esferas adecuadas para administrar fármacos o vacunas mediante inyecciones. En este caso, las nanopartículas administran las instrucciones para que un tipo de células T del sistema inmune se conviertan en células CAR-T. Además, las nanopartículas se han diseñado de manera que el hígado no las elimine, lo que era un requisito y un reto.

Cómo se ha preparado el tratamiento
NANOPARTÍCULAS
Las nanopartículas lipídicas son esferas con una membrana formada por lípidos como la de una célula
En este caso se les ha añadido una proteína a la membrana que les permitirá unirse a células T del sistema inmune y un ARN mensajero con instrucciones genéticas
que se introducirán en las células T
membrana lipídica
ARN mensajero
Proteína de unión con la proteína CD8
de las células T
Paciente
Las nanopartículas se inyectan en el paciente
CÉLULAS T CURATIVAS
El tratamiento se basa en las células T
citotóxicas , que tienen capacidad de
destruir otras células .
Las nanopartículas se unen a la proteína
CD8 que las células T citotóxicas tienen
en su membrana
Proteína CD8
Linfocito T citotóxico
Nanopartícula
El ARN mensajero introduce las instrucciones para que las células T reconozcan las células que deberán destruir. Las células T se convierten así en células CAR-T
ARN
Proteína de unión
con la proteína CD19 de las células diana
Célula
CAR-T
CÉLULAS B PATOLÓGICAS
El objetivo del tratamiento es destruir
las células B que, cuando funcionan mal, causan enfermedades autoinmunes
y algunas leucemias y linfomas
Las células T modificadas se unen a la proteína
CD19 que las células B
tienen en su membrana
y las destruyen
Proteína CD19
Linfocito B patológico
Célula CAR-T
Linfocito B
Fuente: Science
GUYANA GUARDIAN

Cómo se ha preparado el tratamiento
NANOPARTÍCULAS
Las nanopartículas lipídicas son esferas con una membrana formada por lípidos como la de una célula
En este caso se les ha añadido una proteína
a la membrana que les permitirá unirse a
células T del sistema inmune y un ARN
mensajero con instrucciones genéticas
que se introducirán en las células T
Membrana lipídica
ARN mensajero
Proteína de
unión con la
proteína CD8
de las células T
Paciente
Las nanopartículas se inyectan en el paciente
CÉLULAS T CURATIVAS
El tratamiento se basa en las células T
citotóxicas , que tienen capacidad de
destruir otras células
Las nanopartículas se unen a la proteína
CD8 que las células T citotóxicas tienen
en su membrana
Proteína CD8
Linfocito T citotóxico
Nanopartícula
El ARN mensajero introduce las
instrucciones para que las células T
reconozcan las células que deberán
destruir. Las células T se convierten
así en células CAR-T
ARN
Proteína de unión
con la proteína CD19 de las
células diana
Célula
CAR-T
CÉLULAS B PATOLÓGICAS
El objetivo del tratamiento es destruir
las células B que, cuando funcionan mal,
causan enfermedades autoinmunes
y algunas leucemias y linfomas
Las células T modificadas
se unen a la proteína
CD19 que las células B
tienen en su membrana
y las destruyen
Linfocito B patológico
Proteína CD19
Célula CAR-T
Linfocito B
Fuente: Science
GUYANA GUARDIAN

Cómo se ha preparado el tratamiento
NANOPARTÍCULAS
Las nanopartículas lipídicas son esferas con una membrana formada por lípidos como
la de una célula
Membrana lipídica
ARN mensajero
Proteína de unión con la proteína CD8
de las células T
En este caso se les ha añadido una proteína a la membrana que les permitirá unirse a células T
del sistema inmune...
...Y un ARN mensajero con instrucciones genéticas que se introducirán en las células T
Paciente
Las nanopartículas se inyectan en el paciente
CÉLULAS T CURATIVAS
El tratamiento se basa en
las células T citotóxicas , que tienen capacidad de destruir otras células
Proteína CD8
Linfocito T citotóxico
Las nanopartículas se unen a la proteína CD8 que las células T citotóxicas tienen en
su membrana
Nanopartícula
El ARN mensajero introduce las instrucciones para que las células T reconozcan las células que deberán destruir. Las células T se convierten
así en células CAR-T
ARN
Proteína de unión
con la proteína CD19
de las células diana
Célula
CAR-T
Linfocito B patológico
CÉLULAS B PATOLÓGICAS
El objetivo del tratamiento es destruir
las células B que, cuando funcionan mal, causan enfermedades autoinmunes
y algunas leucemias y linfomas
Proteína CD19
Las células T modificadas se unen a la proteína
CD19 que las células B
tienen en su membrana
y las destruyen
Célula CAR-T
Linfocito B
Fuente: Science
GUYANA GUARDIAN

“Es de un extraordinario virtuosismo biotecnológico. Han conseguido algo muy difícil y han hecho la prueba de concepto de que funciona en primates no humanos”, valora Ignacio Melero, inmunólogo de la Clínica Universidad de Navarra. El avance aporta “una enorme esperanza para el tratamiento de enfermedades autoinmunes como lupus eritematoso sistémico”.
Además del lupus, que en algunos casos afecta a órganos vitales y puede incluso ser mortal, otras enfermedades autoinmunes que potencialmente se podrían tratar con células CAR-T incluyen la artritis reumatoide y la esclerosis múltiple.
El tratamiento se ha ensayado en 22 macacos cangrejeros, un modelo animal habitual en investigación biomédica. Los resultados muestran que dos dosis de nanopartículas administradas con tres días de diferencia son suficientes para eliminar casi todas las células B del sistema inmunitario, que tienen un papel decisivo en algunas enfermedades autoinmunes. Estas células B son también la diana de las terapias CAR-T en algunas leucemias y linfomas. Las dos dosis de nanopartículas han sido bien toleradas por los macacos.
El tratamiento con nanopartículas tiene la ventaja de que la eliminación de las células B no es permanente, sino que solo se produce durante un breve periodo después de administrar la terapia. De este modo, se eliminan las células B causantes de enfermedad pero no se eliminarán las células B sanas que el sistema inmune producirá más adelante. Los resultados de los ensayos en macacos “sugieren un reinicio del sistema inmune”, escriben los investigadores en Science.
Otras ventajas de las nanopartículas lipídicas respecto a las células CAR-T producidas en laboratorio es que, al igual que un fármaco, se pueden fabricar en serie y se pueden administrar sin necesidad de una tecnología sofisticada. Por lo tanto, podrían producirse en cantidad suficiente para el enorme volumen de población afectada por enfermedades autoinmunes, algo que no es posible con las terapias CAR-T actuales.
Además, la terapia con nanopartículas no necesita acompañarse de un tratamiento de inmunosupresión.
La investigación tiene como coautor a Ferran Soldevila, inmunólogo catalán formado en la Universitat Autònoma (UAB) y el Royal Veterinary College de Londres, y actualmente científico del equipo de Capstan Therapeutics en San Diego.
Tras los buenos resultados obtenidos en ratones y macacos, la compañía anunció el 11 de junio que ha iniciado un ensayo clínico de un año de duración en el que participarán 38 voluntarios sanos en Australia. Los primeros participantes ya han recibido las nanopartículas con el objetivo de determinar la seguridad del tratamiento y la dosis adecuada. Si los resultados del ensayo son positivos como se espera, se realizarán “estudios de fase 2 para tratar a pacientes con enfermedades autoinmunes”, ha informado Capstan Therapeutics en un comunicado. La compañía no ha precisado qué enfermedades autoinmunes prevé tratar en primer lugar.
Corrección: este artículo ha sido corregido para aclarar que las enfermedades autoinmunes no solo están causadas por las células B. En algunas de ellas, como la diabetes tipo 1, la celiaquía y la psoriasis, las células B también intervienen pero las células T tienen un papel central.